肿瘤磁感应热疗作为新型绿色肿瘤治疗方法,主要利用磁性纳米颗粒的尼尔弛豫 (Néel Relaxation) 和布朗弛豫 (Brownian Relaxation) 等效应,在外加交变磁场的作用下产热,使肿瘤组织快速达到一定的温度而杀灭或诱导肿瘤细胞凋亡,并且磁场穿透深度强,副作用小,更适合深部肿瘤组织治疗与临床转化。一般来说,肿瘤磁感应热疗主要有两个温度窗口。肿瘤组织温度在 50 度以上的磁感应热消融治疗可以非常有效,快速地清除肿瘤,但也容易对周围正常组织造成损伤; 40-45 °C 左右的低温范围可以诱导癌细胞死亡而没有正常细胞受损,但肿瘤细胞会产生对热应激的抵抗力,使得治疗效果大大折扣。因此,探索新的治疗策略具有重要意义。为了克服 42 °C 温和磁感应热疗中肿瘤细胞对热应激的耐受性问题,近日东南大学生物科学与医学工程学院的生物医学纳米技术研究团队在ACS Nano发表“Enhanced Tumor Synergistic Therapy by InjectableMagnetic Hydrogel Mediated Generation of Hyperthermia and Highly Toxic ReactiveOxygen Species”文章(第一作者为博士生武昊安,通讯作者为马明、顾宁和张宇教授),创新性地将Fe3O4纳米酶催化治疗引入到磁感应热疗中,为肿瘤协同治疗提供了新的策略。该工作以PEG和α-环糊精通过包合作用构建具有剪切变稀效应和温敏相转变能力的超分子水凝胶作为治疗平台;以PEI修饰的8 nm Fe3O4纳米颗粒为磁热源和类过氧化物酶;将凝胶注射于肿瘤组织,施加交变磁场使Fe3O4颗粒产热至42 °C,肿瘤组织得到热疗的同时凝胶液化促进凝胶中各组分在肿瘤细胞间隙扩散,并产生较高浓度的H2O2,Fe3O4颗粒在肿瘤微酸性环境中发挥模拟酶功效,通过芬顿反应催化H2O2产生·OH杀伤肿瘤细胞。热疗促进Fe3O4纳米酶酶活性增强而产生更多 ·OH,·OH 进一步损伤热疗中高表达的热休克蛋白HSP 70等,使得热疗效果提升,基于磁性纳米颗粒的磁感应热疗和纳米酶促氧化协同治疗使得肿瘤治疗效果显著,42 °C 温热疗即可消退小鼠乳腺癌皮下瘤。

图1 基于可注射超分子磁性水凝胶的磁感应热和纳米酶催化协同治疗示意图
文章采用双乳液法和超声乳化法分别合成了负载葡萄糖的PLGA纳米胶囊和PFOB携氧纳米乳。高温热分解法合成的Fe3O4纳米颗粒平均尺寸为8纳米,通过配体交换法将DMSA修饰在纳米颗粒表面,然后静电吸附将阳离子聚合物PEI修饰在氧化铁颗粒表面。将PLGA纳米囊和PFOB纳米乳液混合形成溶液A。将α-CD,D-甘露醇和GOD溶解在Fe3O4@PEI胶体溶液中形成溶液B。将溶液A和溶液B以1:1的体积比均匀混合,静置之后即得到可注射器注射的磁性超分子水凝胶。

图2 磁性超分子水凝胶MHZ基本组成及其剪切变稀可注射和温敏相转变特性
水凝胶的酶学性质决定了它产生自由基的能力,MHZ在PFOB纳米乳携带的氧气存在条件下,首先通过水凝胶体相中负载的GOD以生物催化的形式将葡萄糖转变成H2O2,Fe3O4纳米粒子通过在肿瘤微酸性环境下发挥模拟酶功能,可催化H2O2产生高毒性的·OH。为了监测自由基的产生,可将TMB作为显色底物,其被氧化后的产物在650nm波长下显示出可测量的蓝色。研究了不同温度下MHZ的酶催化效果和不同表面修饰的Fe3O4纳米颗粒催化能力不同以及不同葡萄糖浓度范围内MHZ催化能力的变化。
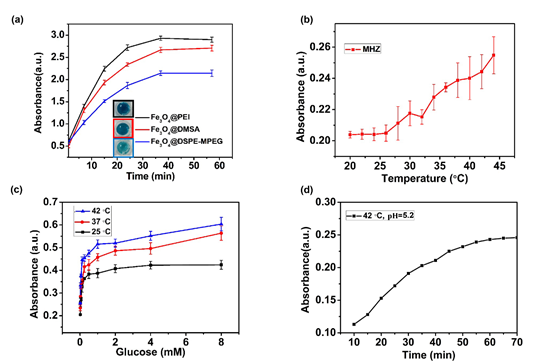
图3 MHZ在体外不同条件下产生羟自由基的催化能力
通常,在肿瘤组织内植入的水凝胶会以其原有形态孤立地存在于组织内,以水凝胶作为磁介质在交变磁场下产生的热量具有较远的扩散范围,可以较全面地覆盖肿瘤组织区域以获得满意的热疗效果; 然而,芬顿反应产生的羟基自由基的杀灭范围只有很短的距离。为了更好地提升磁热与自由基结合时的治疗效果,首先需要解决的是自由基产生的范围问题,即增加肿瘤组织内水凝胶的扩散面积。该文章设计的水凝胶具有温度敏感相变的特殊特征。当温度达到42度相变点时,MHZ变为其溶胶状态并开始在肿瘤细胞之间流动和扩散。此外,D-甘露醇的加入扩大了细胞间隙并进一步促进了MHZ组分在肿瘤组织中的扩散,进而增加了肿瘤组织内的反应范围以获得更好的治疗效果。
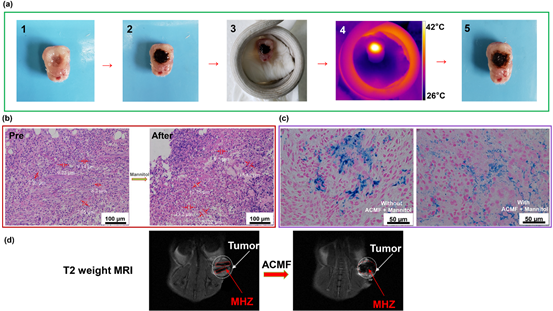
图4 可注射温敏磁性水凝胶MHZ在肿瘤组织中液化扩散实验研究
该文章建立了BALB/c小鼠的4T1乳腺肿瘤模型去验证MHZ的治疗性能。磁性纳米颗粒产生的热量使肿瘤组织温度升高至42℃,给予肿瘤组织42度温热疗的同时致使水凝胶液化,促进纳米颗粒和水凝胶中负载的GOD在肿瘤细胞间隙扩散,水凝胶中负载的甘露醇通过使细胞脱水扩大细胞间隙,增加纳米颗粒在肿瘤细胞间隙的渗透性;此时,GOD和肿瘤组织中富含及PLGA中缓慢释放的葡萄糖反应生成H2O2,与肿瘤组织本身较高浓度的H2O2叠加,Fe3O4颗粒在肿瘤微酸性环境中发挥类过氧化物酶效应,通过亚铁离子和铁离子参与的芬顿反应催化H2O2产生·OH。同时,热疗升温促进Fe3O4纳米酶酶活性增强而产生更多·OH,·OH进一步损伤热疗中高表达的热休克蛋白HSP 70等。治疗后通过记录各个实验组的肿瘤体积,发现MHZ组的肿瘤体积呈现令人满意的根除效果。
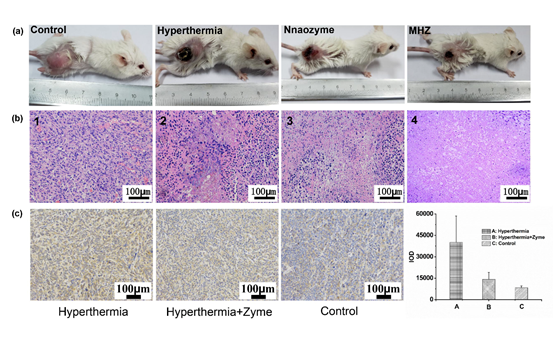
图5 磁热与催化氧化双效应MHZ在体内抗肿瘤效果
本文开发了一种由磁热驱动克服肿瘤内扩散障碍和发挥协同治疗效应的智能可注射超分子水凝胶MHZ。MHZ利用PEG化纳米粒子和α-CD之间的包合作用成胶并且具备剪切变稀可注射性能和42℃相变液化能力。通过小鼠4T1肿瘤治疗试验发现,MHZ可在42℃温和热疗温度下结合纳米酶促氧化的能力,协同治疗消退小鼠肿瘤。这使得长期困扰肿瘤热疗中细胞对热应激的抵抗力问题获得突破的希望。这种由单一纳米颗粒发挥高温和催化疗法的双重功能以协同地治疗肿瘤策略为更安全和精确地协同治疗实体瘤提供了通用平台。后续该研究组将进一步研究和克服肿瘤磁感应热疗中存在的瓶颈,以期为磁感应热疗走向临床提供切实方案。