产品应用案例│银纳米颗粒装饰和介孔二氧化硅涂层单壁碳纳米管增强杀灭耐药细菌的抗菌活性
耐多药细菌引起的感染日益成为全球公共卫生的严重风险,已被世界卫生组织列为对人类健康的最主要威胁之一。不幸的是,新型抗生素药物的开发速度一直在迅速下降,这远远落后于抗生素耐药性的增加。因此,迫切需要探索具有广泛抗菌活性和低耐药性发展倾向的新型抗菌药物。上海交通大学王耀研究组提出了一种新型的抗菌纳米平台,通过N-[3-(三甲氧基硅基)丙基]乙二胺(TSD)介导的方法构建的银纳米颗粒(11 nm,南京东纳生物科技有限公司)装饰和介孔二氧化硅涂层的单壁碳纳米管(SWCNTs@mSiO2-TSD@Ag)(Nano Res.,IF 8.897)。
在本研究中,作者利用该组之前建立的方法合成了具有典型同轴核/壳结构的SWCNTs@mSiO2,外层介孔硅壳能够提高SWCNTs的分散性,从而增加其与细菌细胞壁的接触面积。然后采用TSD介导的策略,通过螯合作用(Ag和TSD之间)和缩合反应(TSD与硅醇基之间),将AgNPs载入SWCNT@mSiO2(SWCNT@mSiO2-TSD@Ag)中。同时,二氧化硅层中大量的介孔作为微反应器,原位合成尺寸小、均匀分布的银纳米颗粒,从而提高抗菌活性。
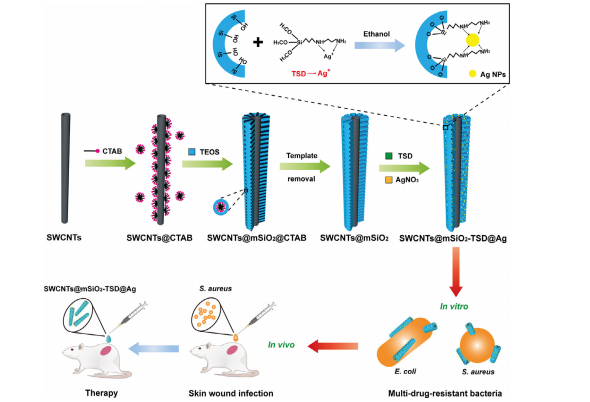
图1. SWCNTs@mSiO2-TSD@Ag的合成示意图
本文重点:
(1)首先,作者通过一系列的表征手段证明了这种新型纳米系统SWCNTs@mSiO2-TSD@Ag中各组分的存在。
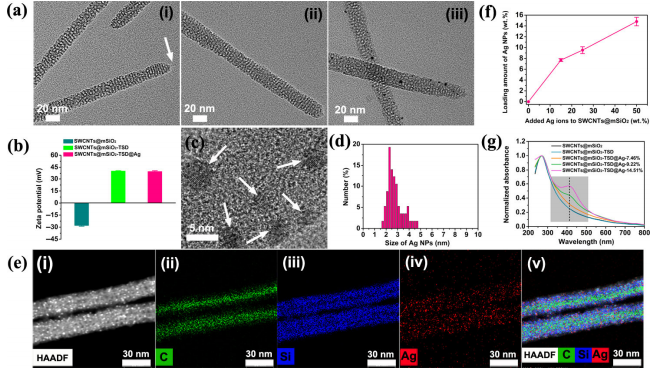
图2. SWCNTs@mSiO2-TSD@Ag的表征图片
(2)其次,选取两株具有代表性的多重耐药菌株,大肠杆菌和金黄色葡萄球菌,评价不同纳米平台的体外抗菌活性。
结果显示,只有当SWCNTs@mSiO2-TSD的颗粒浓度高达925.4 μg/mL时,两种菌株的生长速率才会受到抑制。同时,确定大肠杆菌和金黄色葡萄球菌中AgNPs的最小抑菌浓度(MIC)值分别为14.9μg/mL和31.7μg/mL。相反,对于SWCNTs@mSiO2-TSD@Ag组,当颗粒浓度分别达到120.0和140.0μg/mL时,大肠杆菌和金黄色葡萄球菌的悬液变得视觉透明,表明SWCNTs@mSiO2-TSD@Ag具有显著增强的抗菌作用。此外,通过对细菌生长动力学的研究,进一步证明SWCNTs@mSiO2-TSD@Ag对大肠杆菌和金黄色葡萄球菌的多重耐药菌株的抗菌性能。
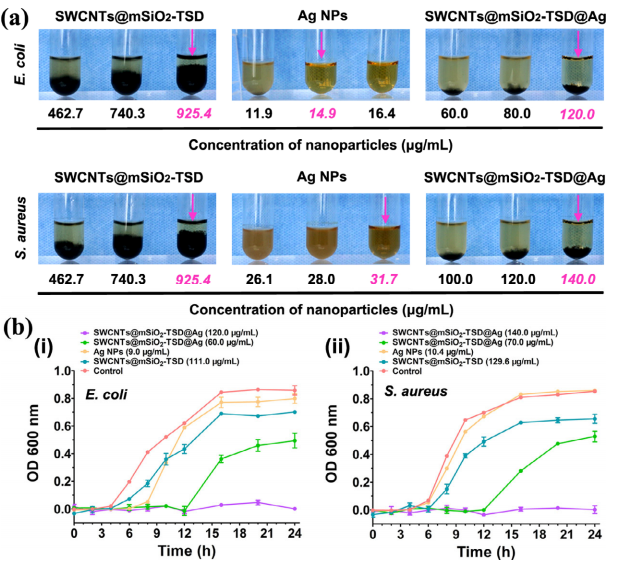
图3. 不同纳米平台的体外抗菌活性评价
(3)利用透射电镜检测了多药物耐药大肠杆菌和金黄色葡萄球菌在不同纳米平台处理后的形态学变化,以评价材料与细菌的相互作用。
结果显示,用SWCNTs@mSiO2-TSD@Ag处理后,可以清楚地观察到材料和细胞膜之间的广泛接触,细胞膜结构严重受损。同时,通过测量不同纳米平台处理耐药金黄色葡萄球菌后的膜电位(用红色通道与绿色通道的荧光比值表示,其中值越低,说明膜电位越小),以进一步表征SWCNTs@mSiO2-TSD@Ag对细胞膜破坏的影响。结果显示SWCNTs@mSiO2-TSD@Ag处理细菌的红/绿色荧光值最小,这些结果进一步证实了透射电镜观察到的结果,即SWCNTs@mSiO2-TSD@Ag纳米平台可能通过破坏细菌细胞膜来发挥其抗菌作用。另外本研究在37°C的水中下检测了相同银含量的AgNPs和SWCNTs@mSiO2-TSD@Ag中Ag+的体外释放行为。结果表明,Ag+主要影响重要蛋白的巯基界面,导致这些酶蛋白失活。Ag+可以限制呼吸链的酶,从而将呼吸控制与ATP合成分离。此外,Ag+还能大大增加细菌中的活性氧(ROS),从而抑制呼吸,诱导GSH的消耗、DNA损伤,最终导致细胞死亡。
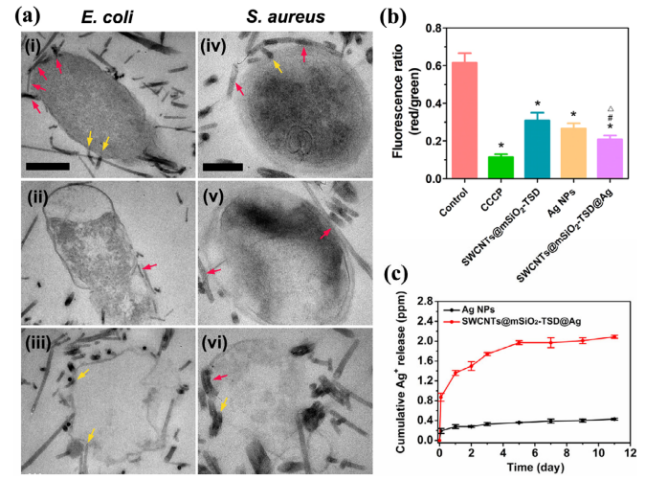
图4. 不同纳米平台与细菌的相互作用评价
(4)采用大鼠皮肤伤口感染模型,评价SWCNTs@mSiO2-TSD@Ag在体内的治疗效果。
选择金黄色葡萄球菌作为皮肤和软组织感染中最常见的病原体进行体内研究。在大鼠背部形成全层皮肤伤口,然后感染多药耐药金黄色葡萄球菌,局部将PBS、SWCNTS@mSiO2-TSD、AgNPs或SWCNTS@mSiO2-TSD@Ag应用在感染的伤口区域,每三天监测一次伤口大小。可以清楚地观察到,经SWCNTs@mSiO2-TSD@Ag处理的感染伤口几乎完全闭合。与SWCNTs@mSiO2-TSD和AgNPs组相比,术后9天的平均伤口大小显著减少。此外,在术后9天进行疤痕宽度的组织学分析,以进一步评估伤口愈合的程度。与对照组相比,三组治疗组疤痕宽度减小,而SWCNT@mSiO2-TSDmSiO@Ag组比SWCNT@mSiO2-TSD或AgNPs组显示出更有效的效果。因此,本研究中的SWCNTs@mSiO2-TSD@Ag纳米平台可以作为一种高效、生物相容性的临床耐药伤口感染抗菌剂。
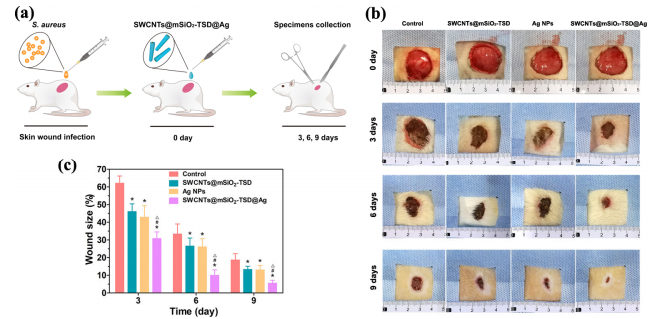
图5. 不同纳米平台对皮肤伤口感染模型的宏观评价
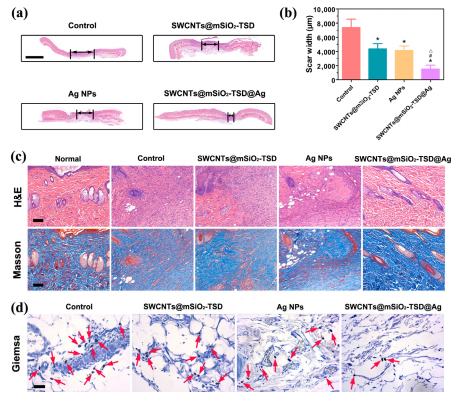
图6. 不同纳米平台对皮肤伤口感染模型的组织学评价
本文总结
本研究利用SWCNTs@mSiO2为宿主载体,以小AgNPs为掺杂粒子,成功开发了一种新型的SWCNTs@mSiO2-TSD@Ag抗菌纳米平台。通过TSD介导的策略,大多数小尺寸的AgNPs在二氧化硅层的介孔内被均匀地装饰。与SWCNTs@mSiO2-TSD和商业AgNPs相比,SWCNTs@mSiO2-TSD@Ag组合纳米系统通过破坏细菌细胞膜和快速释放银离子,对体外多药细菌大肠杆菌和金黄色葡萄球菌表现出更强的抗菌特性。而且,体内大鼠皮肤感染模型验证了SWCNTs@mSiO2-TSD@Ag具有显著提高的细菌清除能力、促进伤口愈合的能力以及良好的生物安全性。因此,这种新型纳米平台在治疗临床耐药感染方面具有广阔的潜力。
参考文献
Zhu Y , Xu J , Wang Y , et al. Silver nanoparticles-decorated and mesoporous silica coated single-walled carbon nanotubes with an enhanced antibacterial activity for killing drug-resistant bacteria. Nano Research, 2020, 13(2):389-400.
“助力科研创新,帮助客户成功”
南京东纳生物科技有限公司
地址:南京市龙眠大道568 号,南京生命科技小镇5号楼,电话:025-83475811
网址:www.nanoeast.net