背景介绍
核酸(DNA或RNA)是最早检测病毒的标志物,对肿瘤的发生、生长有重要的作用。例如,miRNA-21和miRNA-96在早期乳腺癌患者的肿瘤组织和血浆中均表现出明显的失调。重大疾病的早期诊断和治疗迫切需要高水平的低丰度miRNA的超灵敏便携式测量和相应检测策略的创新。其中,侧向流检测法(LFAs)具有操作简单、性价比高、便携、检测时间短等优点。然而,LFAs的灵敏度较低,限制了其在生物医学领域的广泛应用。因此,开发提高侧向流动检测灵敏度的分析方法至关重要。来自于东南大学的刘磊团队采用一种引入了荧光纳米金刚石(FNDs)和金纳米粒子(GNPs)(50 nm及70 nm的GNPs购于南京东纳生物科技有限公司)的复合材料用于miRNA的可视化检测。利用人工智能增强的卷积融合,可以通过色谱和光谱信号的回归分析来确定这些miRNA的类型和浓度。该方法允许在飞摩尔(fM)水平快速检测乳腺癌相关的miRNA-21和miRNA-96,最快可在5分钟内获得结果,R2为0.9916,相关工作发表在ACS Nano(IF=18.02)。
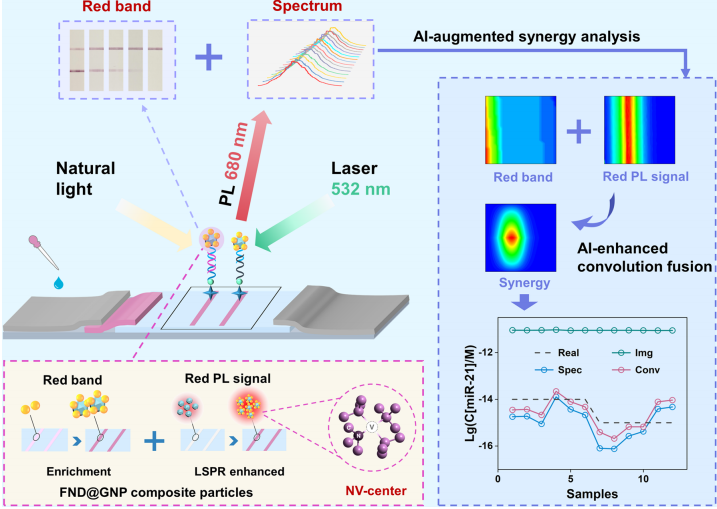
图1、基于双纳米粒子LFAs的人工智能协同增强感知早期疾病诊断示意图
本文重点:
01
FND GNP-SH探针的制备和FND GNP的相互增强
FND GNP双纳米粒子检测系统嵌入到LFA平台中(图1)。利用经典的“三明治法”将待检测的miRNA和相应的FND GNP系统固定在LFA的T线上,可视化和荧光获得的信号可以互相放大。在微波加热辅助方法下,SH探针与GNP共价结合,随后在超声辅助下,GNP-SH-探针与FND静电吸附,形成FND GNP-SH探针。由于FND与GNPs的耦合效应,FND GNP在T线上的视觉呈现会比纯GNPs清晰得多。另一方面,由于GNPs的局域表面等离子体共振(LSPR)引起的荧光增强效应,使得FND GNP在T线上的荧光效果也会优于纯FND。大量的GNPs会在FND表面形成强大的局部电场,加速了受激金刚石的光子释放,同时抑制了非辐射能量的转移。表现为荧光寿命缩短,辐射衰减率增加,荧光强度增强。
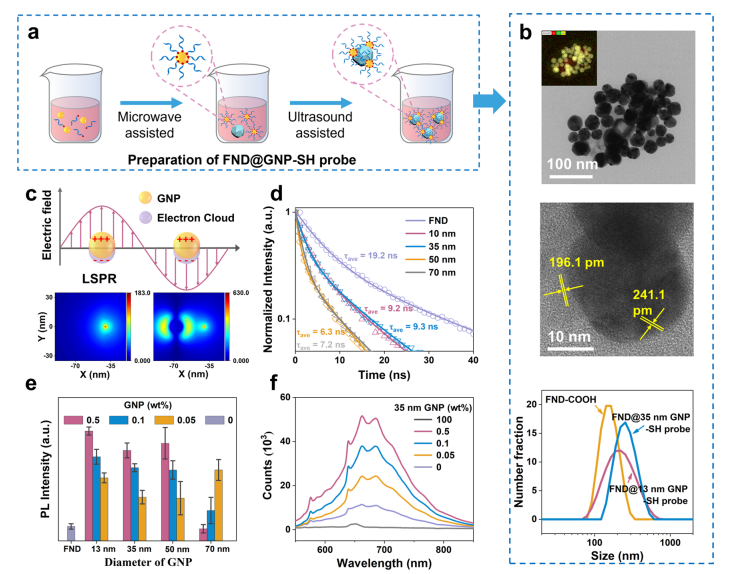
图2、FND GNP双纳米粒子体系的制备及相互增强
02
目视色谱分析
提取的LFA色谱信号的结果可以直接用肉眼观察到,并通过ImageJ软件对相应的照片进行分析。在人工智能辅助色谱分析过程中,首先使用图像处理rgb2ycbcr方法对捕获的图像进行预处理,然后使用支持向量回归(SVR)和高斯过程回归(GPR)进行分析,以帮助确定miRNA浓度。根据以GNPs为载体的LFA上miRNA的测试图片和ImageJ软件的分析结果,可以看到FND GNP在浓度为5 pm时仍能观察到清晰的红色带。
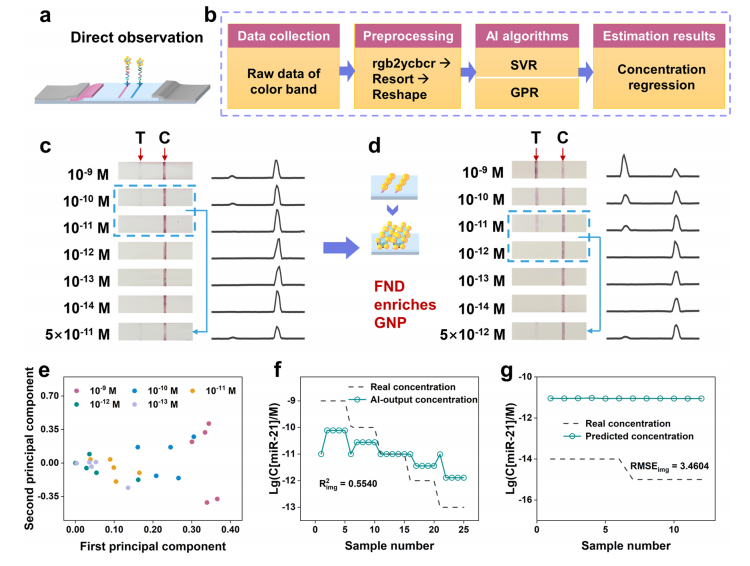
图3、用目视色谱法检测miRNA
03
荧光光谱分析
当待测样品的浓度较低时,可以用荧光法检测到LFA结果。通过荧光法结合LFA,可以检测到LFA结果上的荧光信号,该荧光信号来自于FND中的氮空位(NV)中心。NV中心的能级图反映了FND荧光的产生过程,这有助于理解荧光信号的来源。在LFA中使用FND时,NC膜背景荧光的影响较大,特别是当FND浓度较低时,容易掩盖FND本身的荧光。然而,使用FND GNP作为载体进行测试时,NC膜背景荧光的影响较小,这提高了检测的准确性和灵敏度。通过荧光光谱分析和人工智能技术的结合,可以对miRNA浓度进行分析和预测。该方法对低浓度miRNA的分析效果优于色谱法,具有较好的灵敏度和线性检测能力。
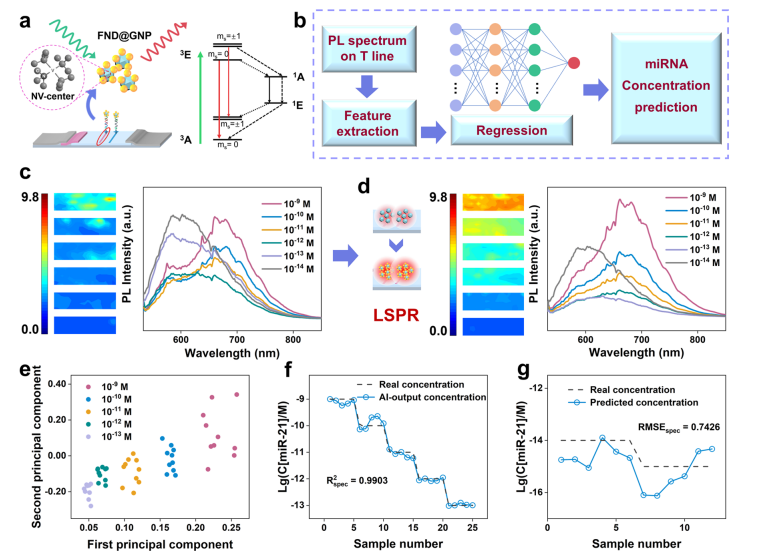
图4、荧光光谱分析检测miRNA
04
AI增强便携式LFA应用
采用人工智能增强技术对便携式LFA进行应用的研究。从LFA的T线收集的色谱和光谱数据经过预处理和信号卷积。随后,使用回归方法SVR和GPR预测miRNA浓度。主成分分析(PCA)结果显示,即使在低浓度10 fM下,也能够明显地区分特征边界。对比分析表明,人工智能增强的协同分析更接近实际结果,并且测试数据集的R2值达到了很高的水平。miRNA-21和miRNA-96作为乳腺癌的重要诊断生物标志物,其检测结果显示出强大的可检测性和特异性。
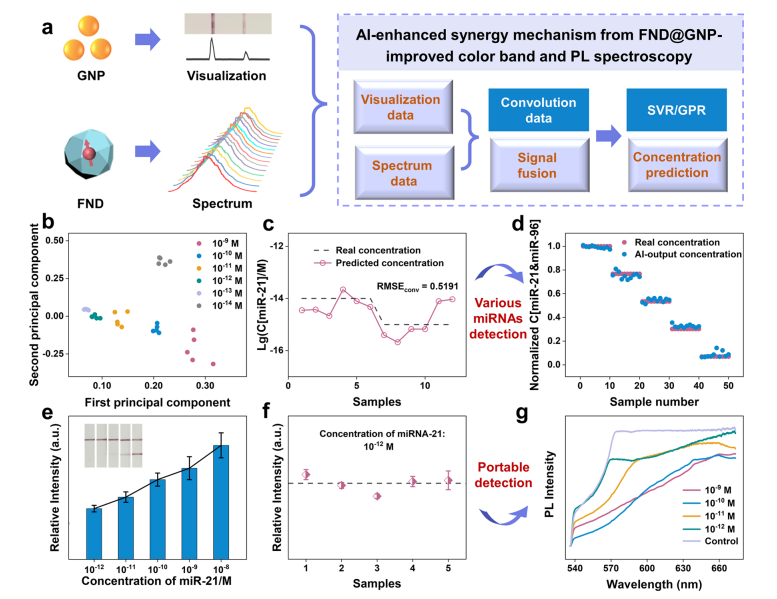
图5、人工智能增强的协同miRNA检测和扩展应用
结论
研究提出了一种协同视觉和光谱技术的人工智能增强的超灵敏生物传感方法。该策略利用了FND GNP双纳米颗粒系统,将其集成到广泛使用的LFA平台中,实现了miRNA的快速、便携式和精确检测。理想情况下,采用上述策略设计的LFA,可以在5分钟内获得fM级别的miRNA的检测结果,且R2值达到了很高的水平。通过在不同的T线上标记早期乳腺癌标志物miRNA-21和miRNA-96的捕获探针,可以同时实现两者的同时检测,检测结果良好。这种方法为恶性肿瘤患者的早期诊断提供了一种新的解决方案。
参考文献:
Wang W.,Liu L.,Zhu J.X.,et.al.,AI-Enhanced Visual-Spectral Synergy for Fast and Ultrasensitive Biodetection of Breast Cancer-Related miRNAs.,ACS Nano 2024,18,8,6266–6275
-END-