Chem. Eng. J.最新综述∣用于肿瘤治疗的纳米药物和纳米材料:进展、挑战和展望
近年来,纳米药物和纳米材料领域迅速发展,在肿瘤治疗方面取得一系列重大突破。然而纳米药物的临床转化仍然面临许多挑战,例如陷入争议的EPR效应、潜在的纳米药物安全风险和复杂制备工艺的纳米药物难以大规模生产等问题。东南大学生物科学与医学工程学院和郑州大学第一附属医院药学部研究人员在Chemical Engineering Journal杂志(影响因子16.744)上发表了题为“Nanomedicines and nanomaterials for cancer therapy: Progress, challenge, and perspectives”的综述文章,东南大学生物科学与医学工程学院博士生、郑州大学第一附属医院药学部主管药师荆自伟为第一作者,张宇教授和张晓坚教授为通讯作者。作者系统总结了纳米药物和纳米材料在肿瘤治疗中的应用进展,主要涉及化学治疗、光热和光动力治疗、放射治疗、化学动力治疗、免疫治疗和联合治疗等。此外,还对纳米药物临床转化存在的挑战进行分析并提出相应的解决策略。
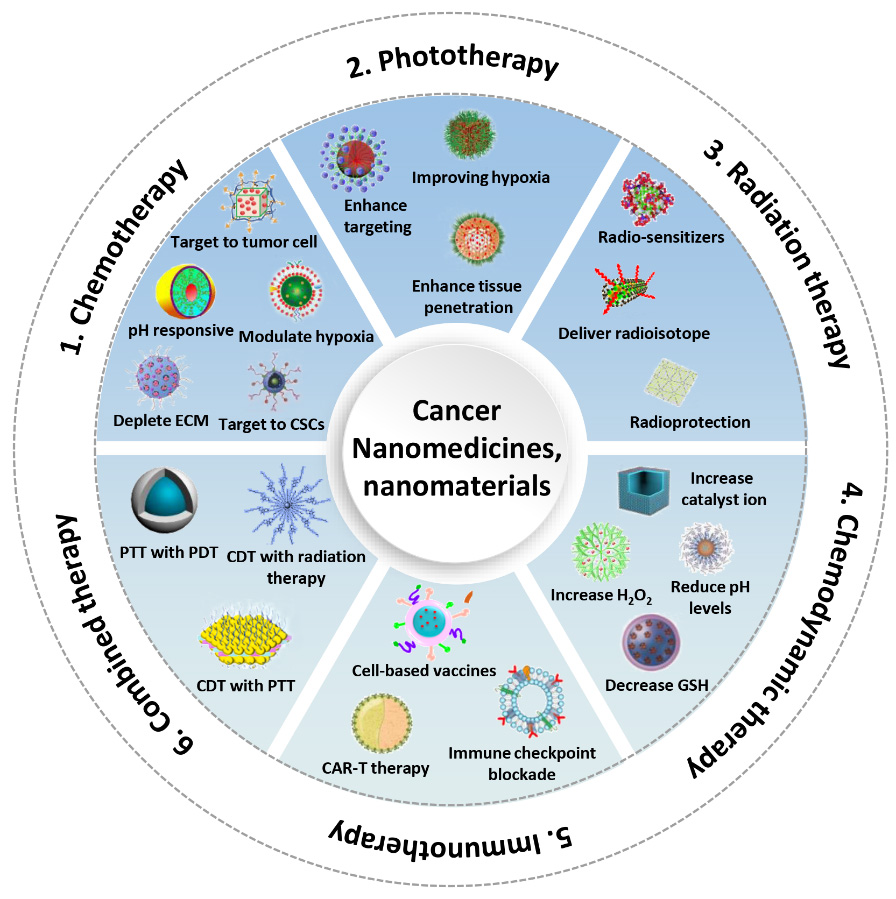
图1.纳米药物和纳米材料用于肿瘤治疗领域的示意图。
针对肿瘤的化学治疗,本文首先总结了靶向肿瘤细胞、肿瘤微环境响应或调控、靶向肿瘤干细胞的纳米药物。其中,肿瘤微环境响应或调控的纳米药物主要包括pH响应(腙键、肼键、亚胺、缩醛等)或pH调节(CaCO3,MnO2和Ca3(PO4)2等),调控乏氧(产氧、运输氧气或者饥饿疗法),使肿瘤血管正常化(阻断VEGFR-2),调节肿瘤相关成纤维细胞,消耗肿瘤基质成分(基质金属蛋白酶、胶原酶、透明质酸酶)等(图2)。
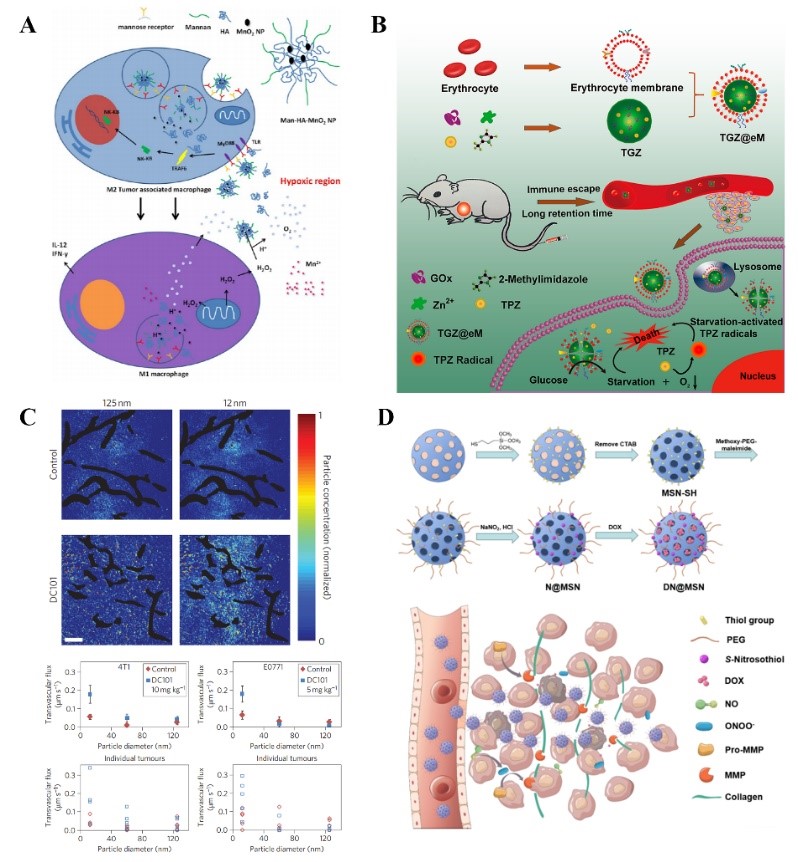
图2.纳米药物通过调节TME用于肿瘤的化学治疗。
纳米材料用于肿瘤的光热和光动力治疗,主要影响因素包括光源、光敏剂和氧。该部分总结了通过被动靶向和主动靶向策略设计的纳米材料用于提高肿瘤组织中的光敏剂含量,通过调节TME中的乏氧状况(改善或恶化)来增强光动力或光热治疗效果。此外,作者还分析了不同光源(NIR-I,NIR-Ⅱ,X射线,和SDT)对治疗效果的影响(图3)。
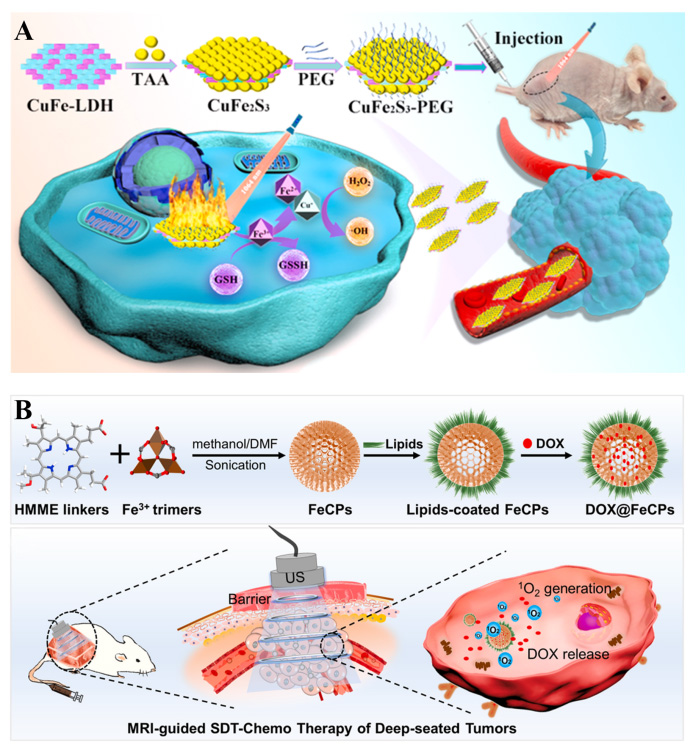
图3.纳米材料利用 NIR-II光源或SDT增强肿瘤的治疗效果。
超过50%的肿瘤患者都曾接受过放射治疗。针对放射治疗中存在的射线吸收差、对正常组织造成损伤、肿瘤缺氧导致的放疗耐受等问题,该部分综述了纳米材料载高Z元素可作为放疗增敏剂用于增强体外放射治疗,或纳米材料递送放射性同位素用于增强同位素内照射治疗。此外,还总结了用于放疗保护的纳米材料(如碳基、铈基、贵金属、TMDC和MXene等)。
考虑到肿瘤TME的特殊性(乏氧、偏酸和过量的H2O2),复旦大学步文博团队提出化学动力治疗,引起了广泛关注。选择合适的纳米材料(铁、铂、铈、铜、锰、钴和石墨烯等)能够增加肿瘤组织中的催化离子数量,从而增强对H2O2的催化效果。此外,通过调控TME环境(增加H2O2含量、降低pH、或者降低GSH水平)也可增强化学动力治疗效果(图4)。
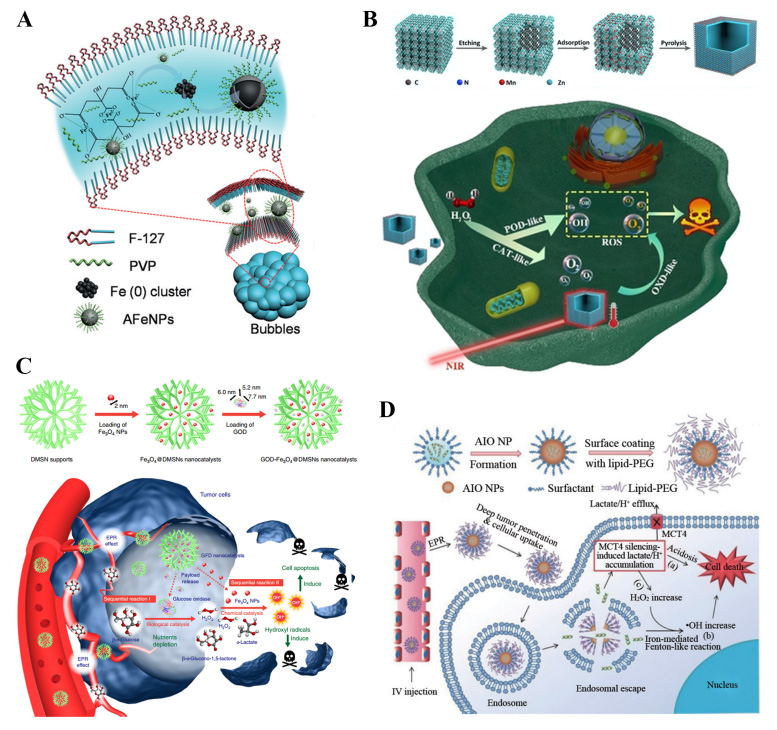
图4.纳米材料用于增强肿瘤的化学动力治疗。
免疫治疗是具有巨大发展潜力的新型肿瘤治疗手段。作者首先对目前的纳米疫苗发展现状进行总结分析,主要包括核酸疫苗(DNA和RNA)、细胞来源疫苗(全细胞、细胞膜、和囊泡等)、新生抗原疫苗、STING激动剂疫苗等。之后,对用于过继免疫治疗的纳米材料进行综述,主要涉及增强CAR-T治疗、仿生抗原呈递细胞和NK细胞等。此外,纳米材料也可用于调控肿瘤免疫微环境,如提高免疫检查点阻断治疗效果、促进肿瘤相关巨噬细胞分化、消耗Tregs和阻断TGF-β信号通路等(图5)。
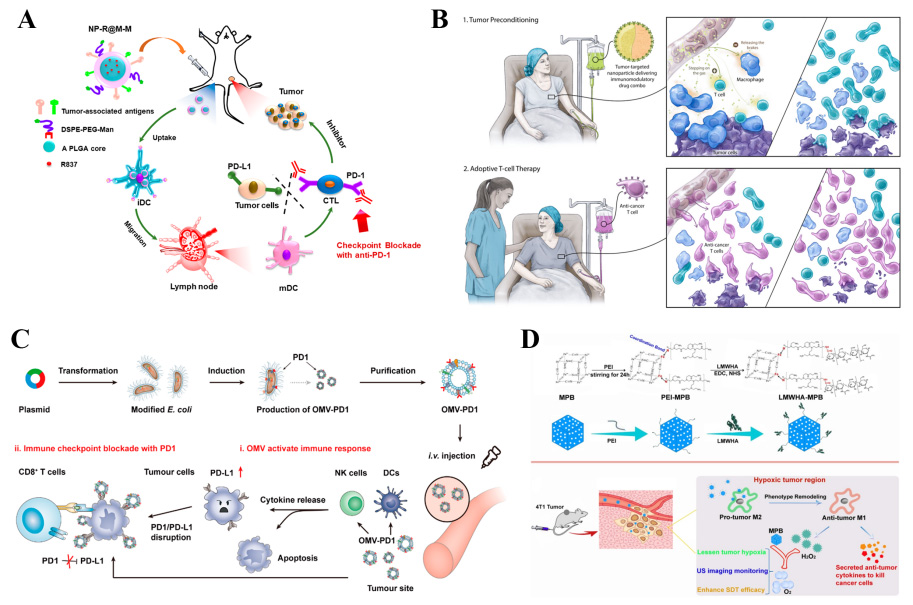
图5.纳米材料用于增强肿瘤的免疫治疗。
此外,本文还总结了纳米药物和纳米材料用于肿瘤的联合治疗,如光热光动力治疗联合化疗、磁疗、化学动力治疗和免疫治疗等。
文章最后,作者对目前肿瘤纳米药物临床转化所面临的问题进行分析,并根据团队工作经验提出可能的解决办法。针对陷入争议的EPR效应,可设计非静脉给药途径的纳米药物;对于潜在的纳米药物安全问题,采用先进策略(如预测毒理学,高通量筛选,多组学和细胞药物动力学、数据挖掘等),以实现“设计安全”的目标;针对复杂工艺的纳米药物难以大规模生产的问题,或可通过设计简单处方、多模态诊疗系统从而实现精准医疗或个体化治疗目标。
该研究受到国家重点研发计划和国家自然科学基金等项目的支持。
文章链接:https://doi.org/10.1016/j.cej.2022.137147